Since I love author blog posts about papers, I thought I’d write a little about papers I’ve contributed too. So far, they’re not that many, but maybe it can be a habit.
”Heritable genome-wide variation of gene expression and promoter methylation between wild and domesticated chickens” was published in BMC Genomics in 2012. The title says it very well: the paper looks at differential expression and DNA methylation of a subset of genes in the hypothalamus of Red Junglefowl and domestic White Leghorn chickens. My contribution was during my MSc project in the group. Previously (Lindqvist & al 2007; Nätt & al 2009) Daniel Nätt, Pelle Jensen and others found a transgenerational effect of unpredictable light stress on domestic chickens. After that, and being interested in chicken domestication, a DNA methylation comparison of wild and domestic seems like a natural thing to do. And it turns out Red Junglefowl and White Leghorns differ in expression of a bunch of genes and in methylation of certain promoters (where promoter is operationally defined as a region around the start of the gene model). And when looking at two generations, the contrasts are correlated between parent and offspring. There is some heritable basis of the differences in gene expression and DNA methylation.
In Red Junglefowl, ancestor of domestic chickens, gene expression and methylation profiles in thalamus/hypothalamus differed substantially from that of a domesticated egg laying breed. Expression as well as methylation differences were largely maintained in the offspring, demonstrating reliable inheritance of epigenetic variation.
What I did was methylation sensitive high resolution melting. HRM is a typing method based on real time PCR. After PCR you often make a melting curve by ramping up the temperature, denaturing the PCR product. The melting characteristics depend on the sequence, so you can use melting to check that you get the expected PCR product, and it turns out that the difference can be big enough to type SNPs. And if you can type SNPs, you can analyse DNA methylation. So we treat the DNA with bisulfite, which deaminates cytosines to uracil unless they are protected by methylation, and get a converted sequence where an unmethylated C is like a C>T SNP. We set up standard curves with a mixture of whole-genome amplified and in vitro methylated DNA and measured the degree of methylation.
That is averaging over the population of DNA molecules in the sample; I’ve been wondering how HRM performs when the CpGs in the amplicon have heterogenous methylation differences. We’ve used HRM for genotyping as well, and it works, but we’ve switched to pyrosequencing, which gives cleaner results and where the assay design is much easier to get right the first time. I don’t know whether the same applies for methylation analysis with pyro.
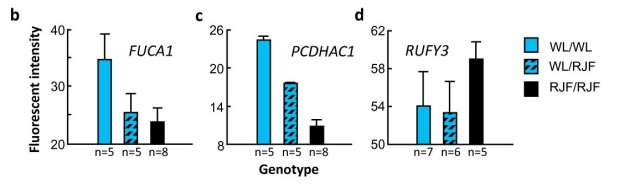
My favourite part of the paper is figure 4b (licence: cc:by 2.0) which shows methylation analysis in the advanced intercross of Red Junglefowl and White Leghorns, which immediately leads to, as mentioned in the paper, the thought of DNA methylation QTL mapping.
Literature
Nätt, D., Rubin, C. J., Wright, D., Johnsson, M., Beltéky, J., Andersson, L., & Jensen, P. (2012). Heritable genome-wide variation of gene expression and promoter methylation between wild and domesticated chickens. BMC genomics, 13(1), 59.
Lindqvist C, Janczak AM, Nätt D, Baranowska I, Lindqvist N, et al. (2007) Transmission of Stress-Induced Learning Impairment and Associated Brain Gene Expression from Parents to Offspring in Chickens. PLoS ONE 2(4): e364. doi:10.1371/journal.pone.0000364
Nätt D, Lindqvist N, Stranneheim H, Lundeberg J, Torjesen PA, et al. (2009) Inheritance of Acquired Behaviour Adaptations and Brain Gene Expression in Chickens. PLoS ONE 4(7): e6405. doi:10.1371/journal.pone.0006405